29/6/22 水和水をもつ物質の溶解度は,無水物の量で表されるので,溶解度の計算は少し複雑になります。 問題を解いて考えてみましょう。 学習アドバイス 水和水を含む結晶の溶解では,水に解けたときに水和水が溶媒の一部になるのでややこしく感じ30/6/22 70℃で135g溶解している飽和水溶液を30℃まで冷却すると,30℃では45gしか溶解できないので 135-45=90g析出します。 また,70℃のときの飽和水溶液は100+135=235gです。 以上より, 「70℃→30℃の冷却では,飽和水溶液235gにつき,90g析出する」亜鉛鉱としては閃亜鉛鉱 (ZnS) や菱亜鉛鉱 (ZnCO 3) が主要であり、日本の亜鉛鉱山は閃亜鉛鉱が主である。細かく破砕された鉱石から浮遊選鉱などで脈石・銅鉱物・鉛鉱物などを分離したものは亜鉛精鉱と呼ばれる(亜鉛含量 5058 %)。 亜鉛精鉱は焼結により団塊とされることが多い。

濃度の計算の人気動画を探索しましょう Tiktok
水溶液の計算問題
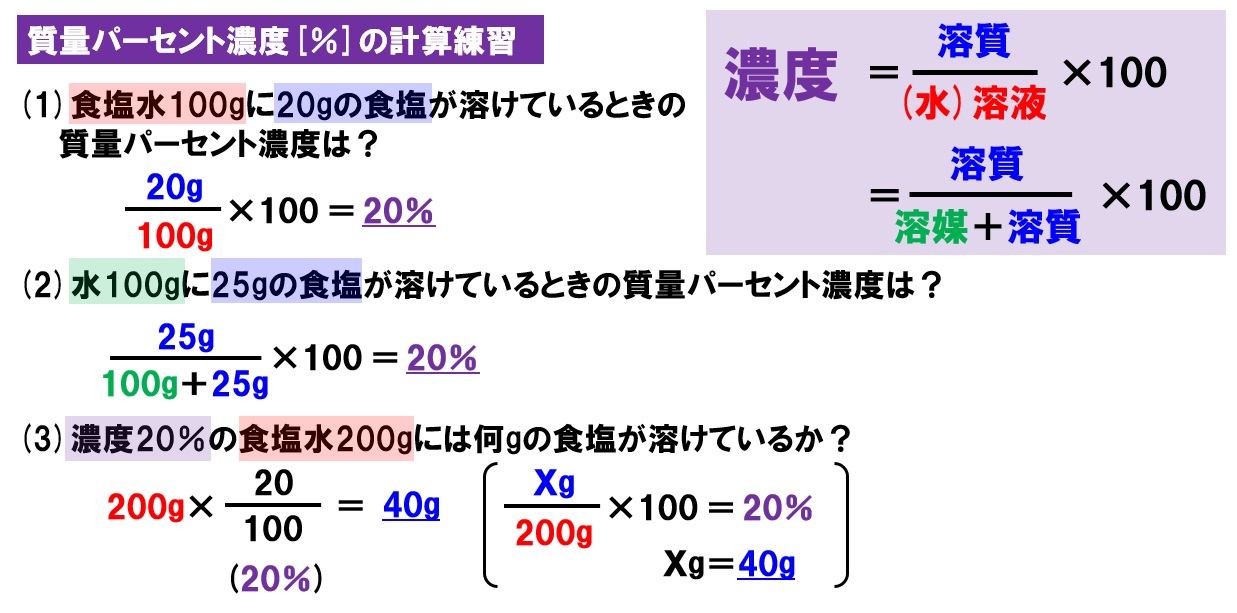
水溶液の計算問題-質量パーセント濃度 質量パーセント濃度 (%)= 溶質の質量 (g) 溶液の質量 (g) ×100 例 90gの水に10gの塩化ナトリウムをとかしたら、 100gの塩化ナトリウム水溶液になる。 このとき 溶質10g, 溶液 (溶媒溶質)100gなので 濃度は 10 100 ×100=10 (%) 塩化ナトリウム 100g 90g 10g 水 塩化ナトリウ Re気相濃度と水溶液の濃度の計算について Lake (ZWla752 水溶液濃度1ppmは重量分率、気相中濃度1ppmは体積分率、気体を理想気体と仮定すると体積は分子数(モル数)に比例する(もちろん温度、圧力一定で)・・・ この辺から計算式は作れ




中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu
もくじ 1 緩衝液の役割:pHの変化をゆるやかにする 11 電離定数を利用し、緩衝液のpHを計算する;7/4/ 中学1年理科。水溶液と濃度について学習します。 レベル★★★☆ 重要度★★★☆ ポイント:濃度の計算方法授業用まとめプリントは下記リンクからダウンロード!授業用まとめプリント「水溶液と濃度」水溶液とは水溶液とは、物質が水に溶けたもので5/6/15 水溶液の濃度にまつわる練習問題 解答 %の食塩水、 %の砂糖水といった、水溶液の「濃度」についての計算問題プリントです。 苦手な人が多いけど、しっかり身につけよう! 数学でも役に立つ場面があるよ (^ ^) 溶解度曲線の見方 練習問題 No 1 溶解
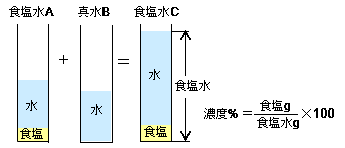
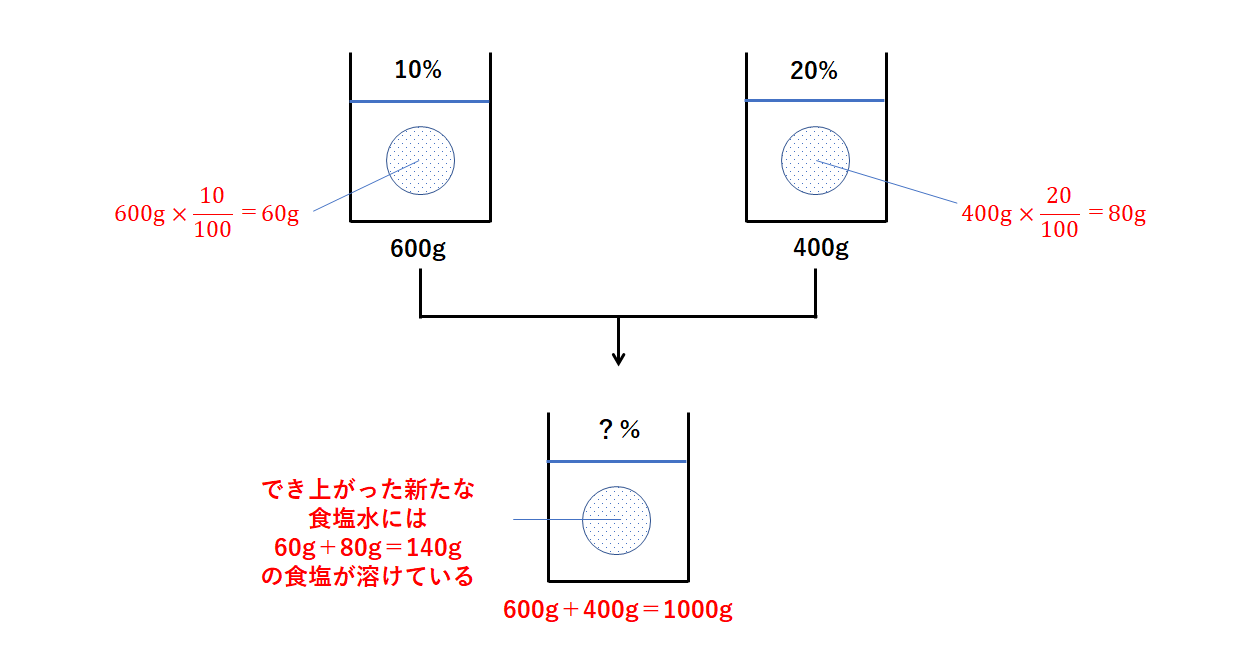
星の王子 さん 水より重い液体に適用される式です。 d = 1443/(1443 - Bh) d : 15℃水溶液の 比重(4℃の水を規準として) Bh : 15℃水溶液の ボーメ度 この式は元々 実験式ですし、また式の成り立ちから見ても計算結果の有効数字は 3桁か、せいぜい 4桁 と考えるべきです。G Cの濃度 % (1) Aの食塩=Aの食塩水×Aの濃度 (2) Bの食塩=Bの食塩水×Bの濃度 (3) Cの濃度=Cの食塩÷Cの食塩水 = (A+Bの食塩)÷ (A+Bの食塩水) お客様の声溶液中の水が電気分解される前と、後とで同じものは硫酸の質量です。 電気分解された水の質量を とすると、 電気分解された後の溶液の質量は なので ( 10% 中の硫酸の質量)=( 11% 中の硫酸の質量) として方程式を立てると より (g) 比重を利用する溶液の計算問題 今さらいう必要はないと思いますが「比重」は水に対する質量だと考えてかまいません。 水の密度は です。 比重をかければその物
さらにlog 10 2=030、log 10 3=048とし、今回の水溶液の体積は常に10Lで変わらないものとする。 塩酸を加える前の水溶液は先ほどの問題の緩衝液で、このpHは474でした。この緩衝液に塩酸という強酸を加えたときにpHがどのように変化するか計算していき水溶液の濃度計算まとめ ①溶解度=水100gに物質がとける最大の重さ ②水溶液の濃度=水に溶けた物質の重さ÷(水の重さ+水に溶けた物質の重さ) =水に溶けた物質の重さ÷水溶液の重さ17/2/19 水酸化カルシウム アルカリ性 水酸化ナトリウム水溶液 水酸化ナトリウム アルカリ性 溶質の名前がそのまま使われている水溶液が多いですね。 ただし、食塩をとかした場合には塩化ナトリウム水溶液というので覚えておきましょう。 また、石灰水は




質量パーセント濃度の計算問題集 基本編 Menon Network



受験化学 9 溶解度の計算1 みかみの参考書ブログ
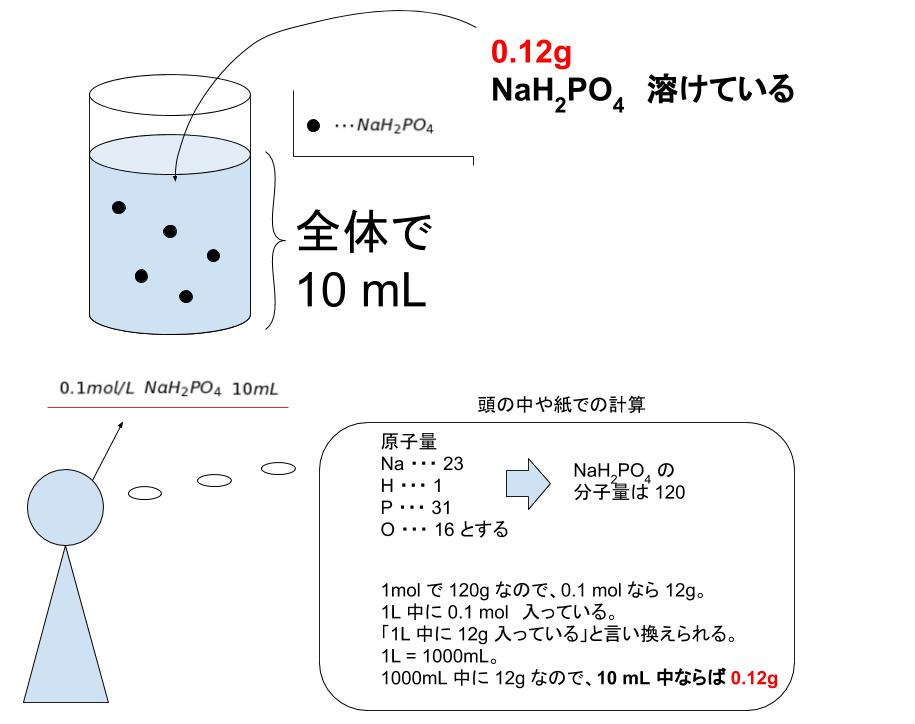
次に質量パーセント濃度を計算しましょう。先に説明した通り、1Lの水溶液がある場面を想定します。 1L(=1000cm 3 )の水溶液の重さはいくらでしょうか。水溶液の密度は11g/cm 3 なので、1Lの重さは1100gとわかります。 \(11×1000=1100\)17/4/03 xmol/lの水溶液を1リットル作る場合、硫酸銅5水和物xモルを、水〔1000- (5x×18)〕に溶解させなくてはいけません。 ここで1000は水1リットルの重量、 (5x×18)は硫酸銅5水和物に含まれている水の重量です。 この溶液をyml作る場合には、溶質、溶媒とも (y/100026/1/22 質量パーセント濃度は計算で求めます。 計算式は 質量パーセント濃度 (%) = (溶質の質量 (g))÷ (水溶液の質量 (g)) ×100 ということでまた問題! 問② 砂糖を10g入れてつくった砂糖水が100gある。 この砂糖水の質量パーセント濃度は? 今度もできましたか? 正解は 式:10 ÷ 100 × 100 答え:10% ちなみに、水溶液の質量は 溶媒の質量 + 溶質の質量 なので 質量パーセント濃度 (%)



中1理科 水溶液と濃度 水溶液の性質と濃度計算 Pikuu




中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu
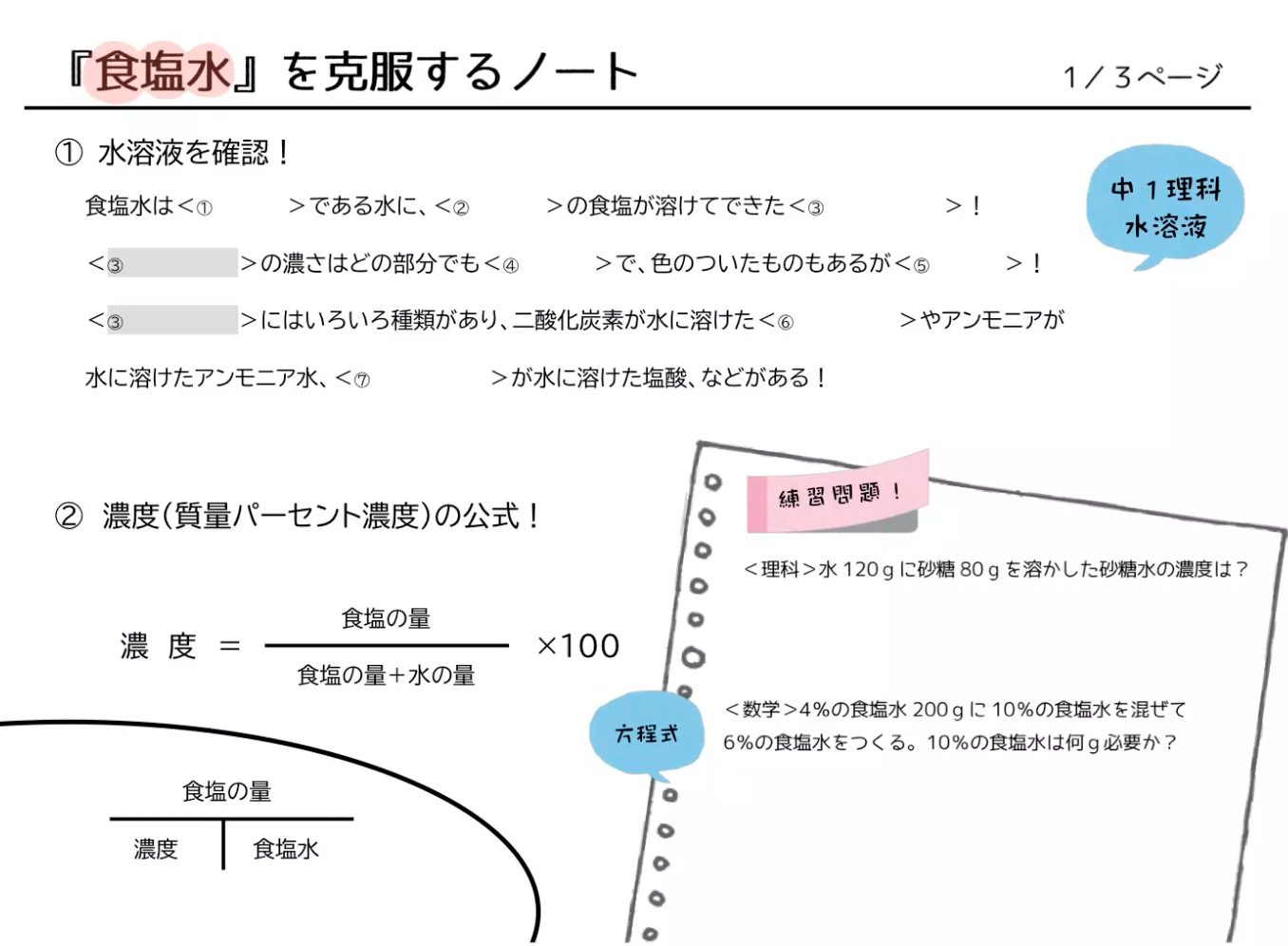
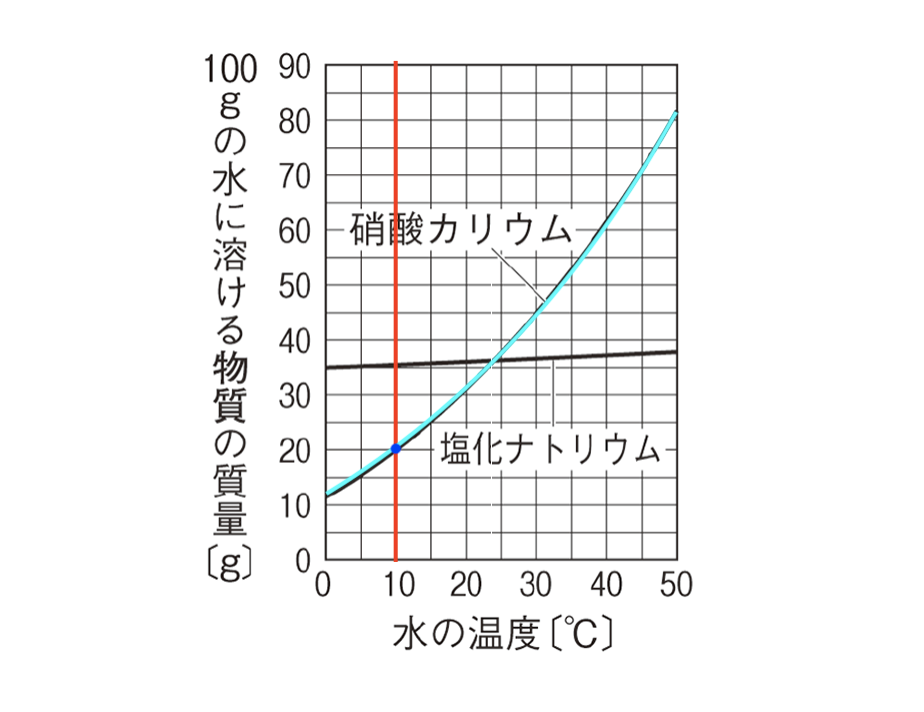
2 不完全な中和反応によって生じる緩衝液の計算 21 電離定数を利用し、塩の水溶液のpHを求める; 溶解度曲線を使った問題 下の図は、3種類の物質A~Cについての溶解度曲線です。 このとき、次の問いに答えなさい。 (1)60℃に水100gに最もよく溶ける物質はA~Cのどれか。 (2)60℃の水100gに物質A~Cをそれぞれ溶解度まで溶かし、それらの水溶液を30℃まで24/4/16 水溶液の濃度(質量パーセント濃度)の公式と求め方:食塩水の濃度を計算するやり方 24 April 16 水溶液の濃さは溶質の質量を水溶液の質量で割って 100 をかけて求めます。 濃度(%)=溶質の重さ(g)÷水溶液の重さ(g)×100 この値を質量パーセント濃度ともいいます。 単に濃さという場合は、この質量パーセント濃度を指します。 パーセントという名前がついているよ




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく
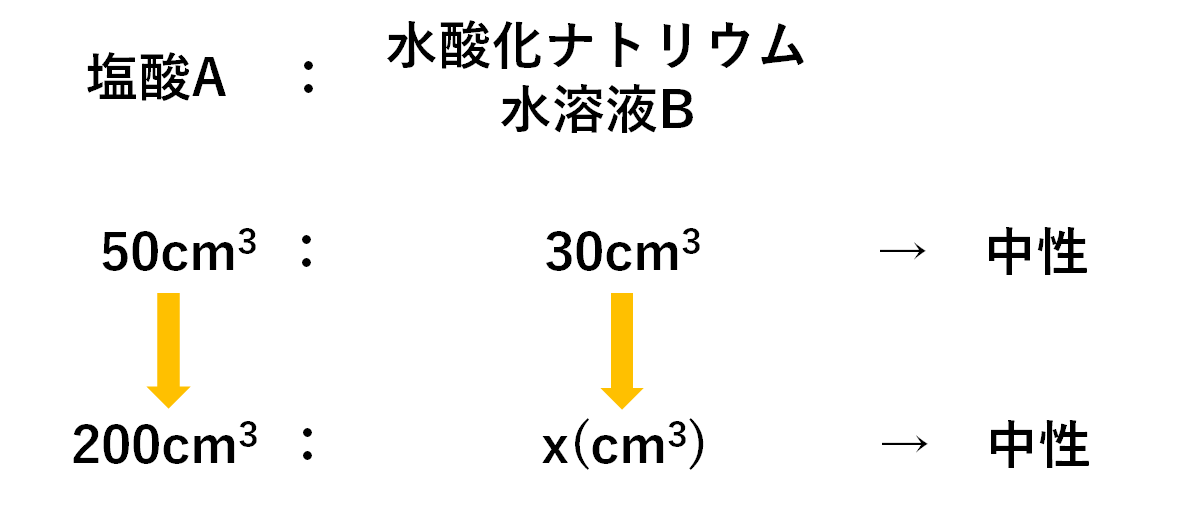



中3化学 中和の量的関係 中学理科 ポイントまとめと整理
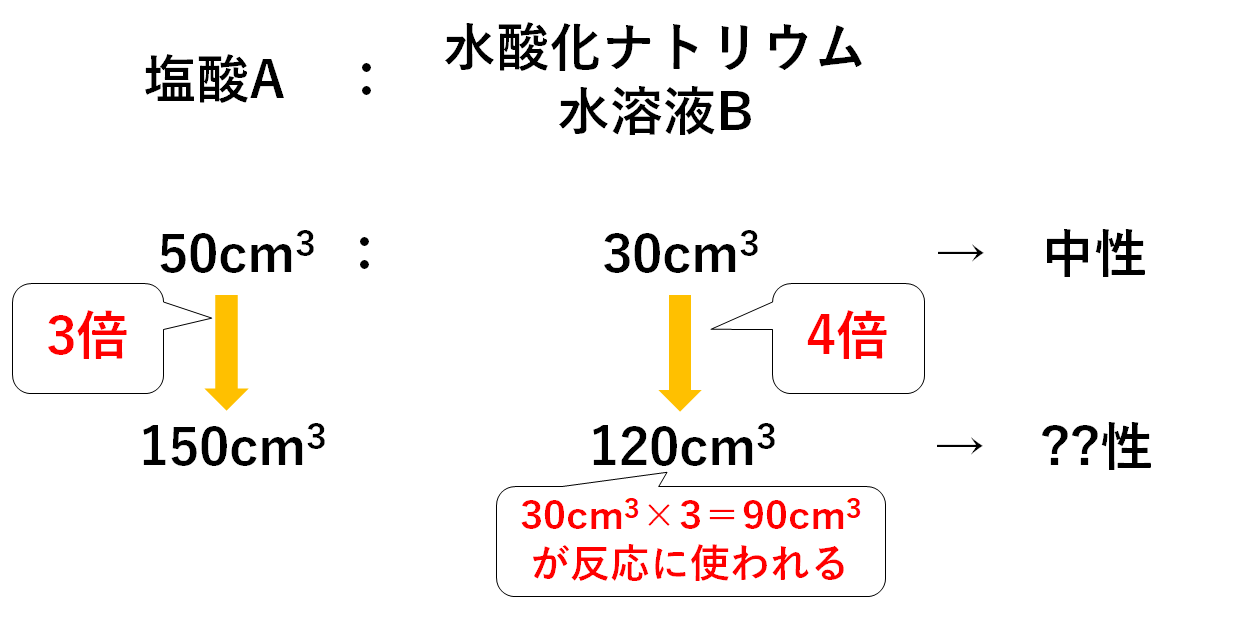
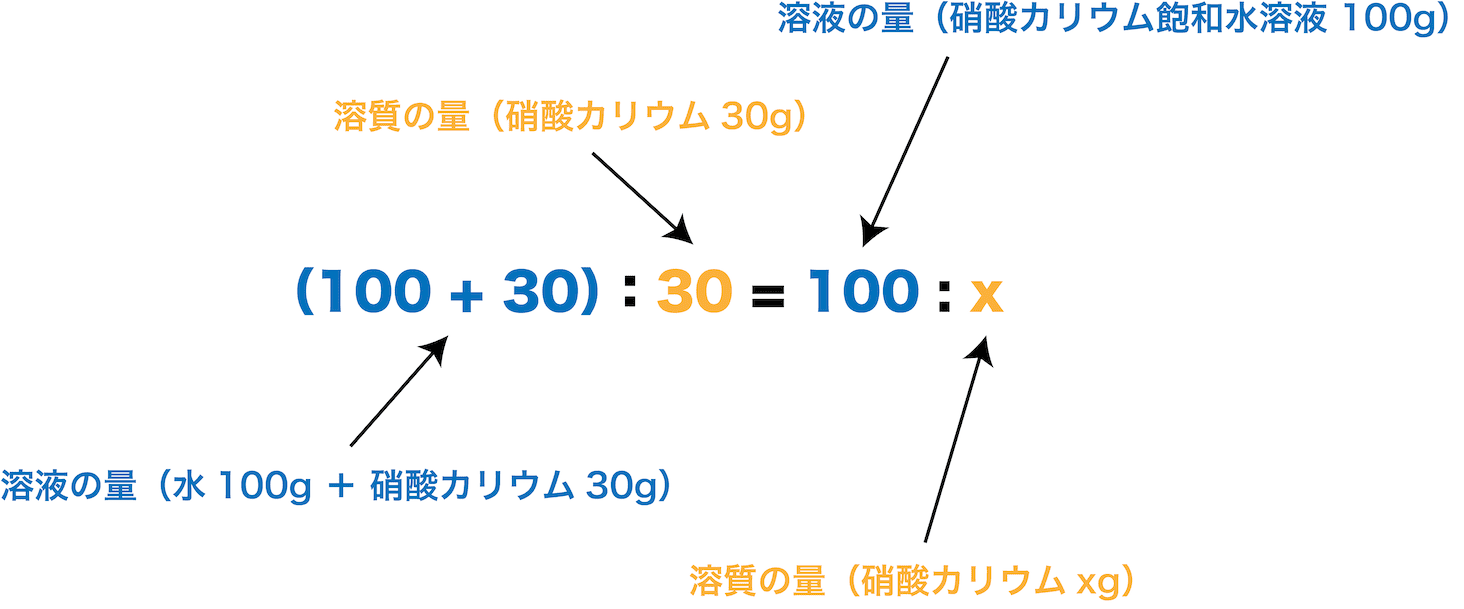
溶液の比で計算します。 80 ℃は同じなので見なくて良い問題ですね。 溶解度が 51 なので、100g の水に 510g の塩化カリウムが溶けるということなので、 溶液 151g 中に 510g の溶質が溶けています。 これを利用して比をとります。 「溶液 151g 中に 510g の溶質、溶液 100g 中には何gの溶質? 」 という比例式です。 飽和溶液 100g 中に溶けている塩化カリウムの質量を とすると これは問題に6/4/21 まずは解説動画をご覧ください↓ ① 塩の加水分解と弱酸遊離の原理(弱酸の性質によって起きる現象) ② 中和の計算を極める問題(複数の反応を扱った問題の解法、弱酸(弱塩基)遊離→逆滴定) ③ pHの計算(対数を使った計算、pOHとの関係、水の5/8/17 H 2 SO 4 は 2価の酸 なので、含まれているH の物質量(mol)はH 2 SO 4 の物質量(mol)の2倍。 したがって 1 ( m o l) × 2 = 2 ( m o l) このようになる。 つまり、酸がもつH の物質量(mol)は 「酸の物質量(mol)×酸の価数」 で求めることができるということである。 同様に、塩基がもつOH – の物質量(mol)は 「塩基の物質量(mol)×塩基の価数」 で求めること




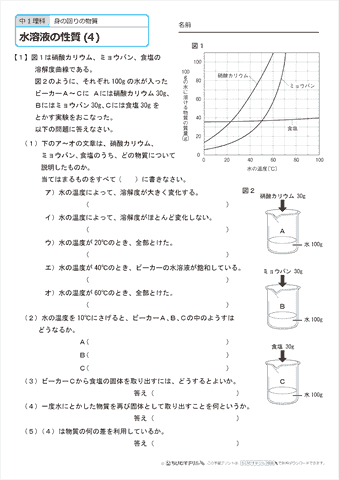
中学1年生 理科 水溶液の性質 練習問題プリント 無料ダウンロード 印刷 ちびむすドリル 中学生




オンライン講座 個別指導 プロが教える理科講座 ものの溶け方の計算 By 川野 ゆみ ストアカ
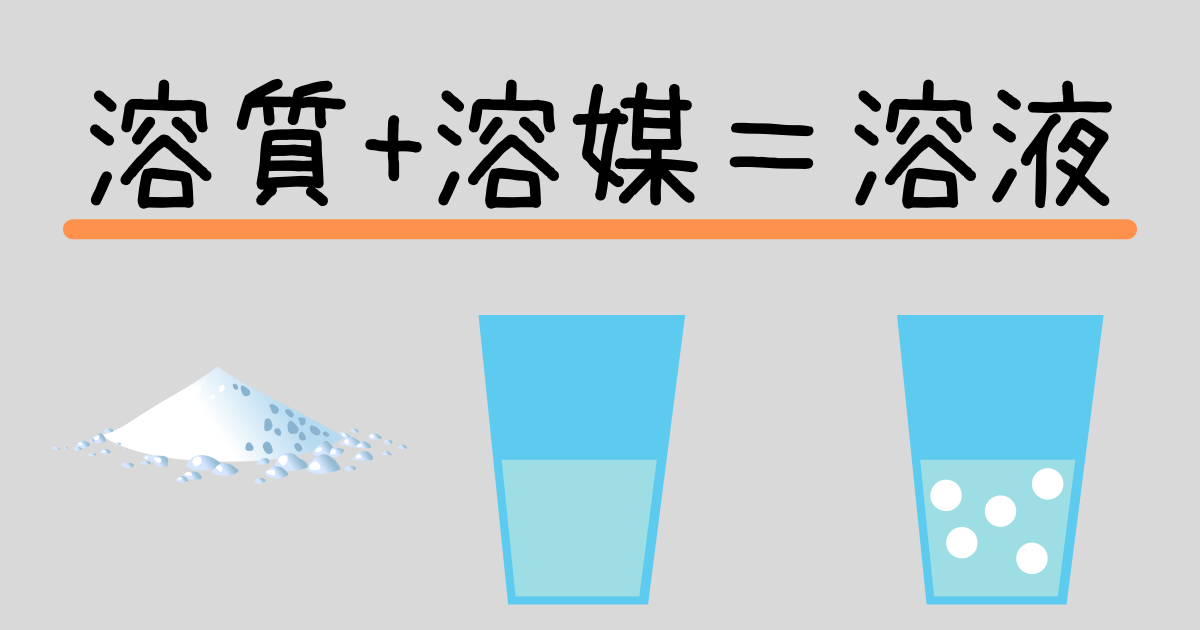
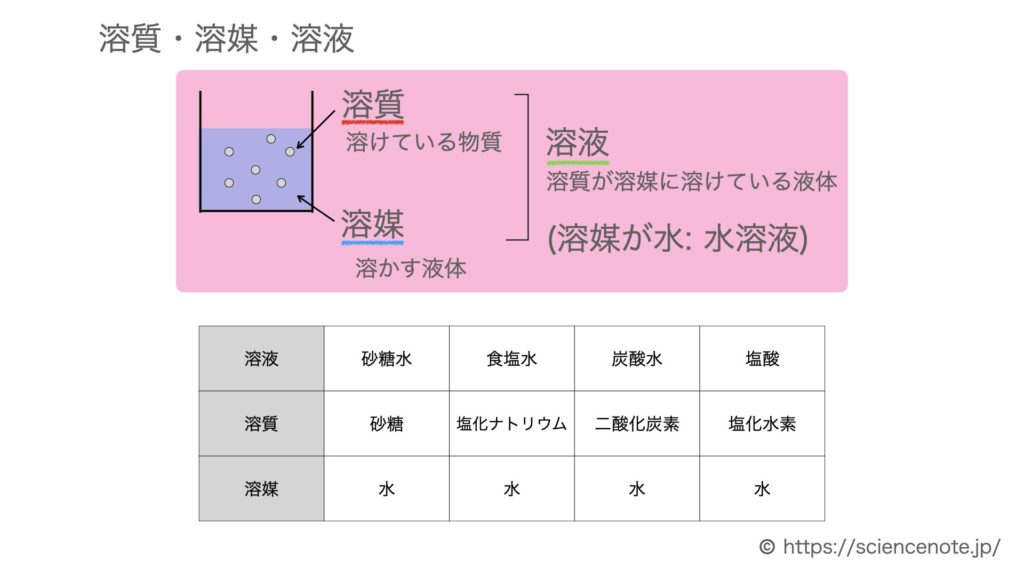
溶液と溶液の濃度 (1) 溶液 溶液 : 成分物質が互いに均一に混じり合っている液体。溶質と溶媒からなる。 溶質 : 液体に溶けている物質 例) 塩水(NaCl水溶液)の塩(NaCl) 溶媒 : 溶質を溶かすような物質 例) 塩水(NaCl水溶液)の水 水溶液の勉強法 水溶液の学習において次のことが大切です。 濃度の式・溶質の質量の式はしっかり覚える 濃度を求める式・溶質の質量を求める式はしっかり覚えましょう。 もう一度書いておきます。 「濃度(%)」=(「溶質の質量(g)」÷「溶液の質量(g)」)×100 結晶が出るとき水溶液は飽和している。 25度の水溶液の中にXは限界一杯の6g 溶けています。 そして溶けきれなかったXの結晶が45g あります。 混合粉末にあったXの量=45+6=51g 85% 固体が溶けた水溶液は水の温度を上げるとふつう溶解度は大きくなります。




モノマナビ研究所




中学受験理科講座 水溶液の濃さと溶解度
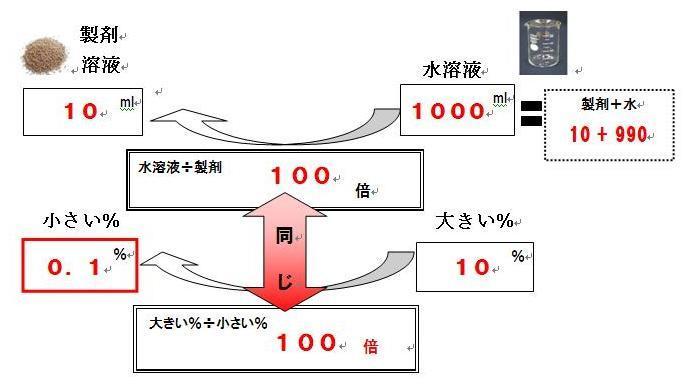
9/2/17 ①と②より、水酸化ナトリウム水溶液1Lを仮定した時の水酸化ナトリウムNaOHの質量と水酸化ナトリウム水溶液の質量が計算できました。 よって、求める質量パーセントは、 56g / 1400g × 100 = 4%・・・(答) となります。 いかがでしたか?1/1/18 濃度 (%)中心に薬液量計算を行う方法 ※わからない部分はXとする ※原液の濃度 (%)×薬液量 (ml)=希釈液の濃度 (%)×希釈液量 (ml) 上記の計算方法に当てはめると、10%塩化ナトリウム水溶液の必要な量がわかっていないので、 10×X=02×500 10X=100 X=10 となり、答えが10mlと出ま①調整後の水溶液の量→ 原液の量 と希釈に用いる 水の量 を足すと求めることができます。 ( 5ml 995ml =1000ml) ②調整後の水溶液の%→この値( X とする)を求め、実際に美容所で使用できる濃度なのかを確かめていく。




水溶液濃度 ちょっと厄介な2問題と解法 制限2問で7分 中学 数学 理科の復習サイト




Pdf 濃度の計算ドリル45題 中学理科ポイントまとめと整理 オンラインショップ
10/5/ ID非公開 さん /5/10 2133 2 回答 水溶液の密度の求め方について。 例えば、Aグラムの硫酸ナトリウムをBグラムの水に溶かした水溶液の体積がC mlのときの水溶液の密度 (g/cm³)はどう求めたら良いのでしょうか? 質量というのは、溶質なのか溶媒なのか溶液の濃度計算と調製方法のインターネットによる自動サービス -塩化ナトリウム水溶液- 芦田実*,五十嵐真由美,務台ひろみ,吉田俊久 埼玉大学 教育学部 〒 埼玉県さいたま市桜区下大久保255 Email ashida@postsaitamauacjp定義・説明 ppm parts per millionの略。 百万分率。 を1単位として割合をみる場合の「単位」と考えてもよい。 1ppm= =10 4 % 溶液の濃度をppmで表す場合は、 ppm= 希薄水溶液では、密度を1 g/ml として溶液の質量を求める。




質量パーセント濃度の計算問題集 基本編 Menon Network



中3化学 中和の量的関係 中学理科 ポイントまとめと整理
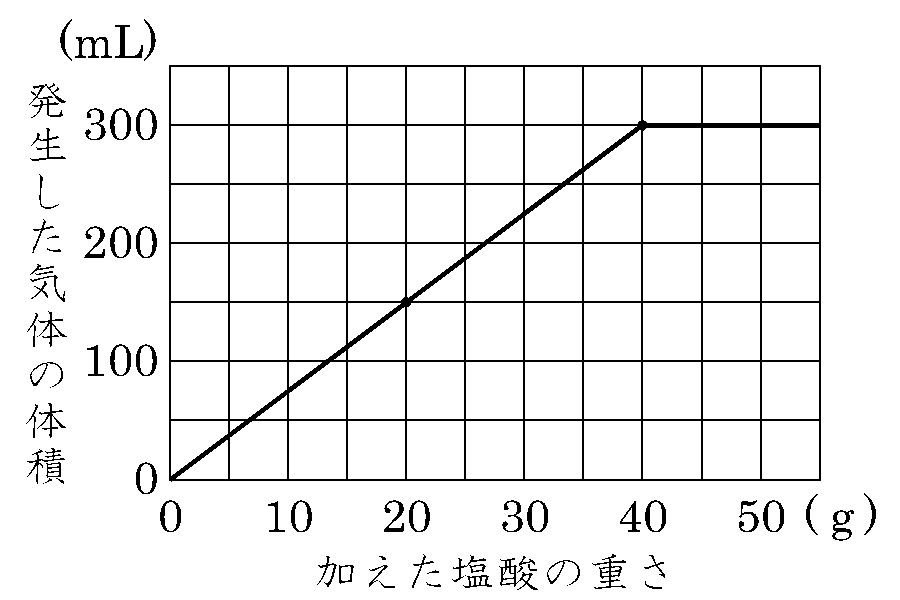
計算式 必要な原液量 (mL)=希釈液の濃度 (%) / 原液の濃度 (%) × 作成する希釈液の量 (mL) 必要な原液量 (mL)=作成する希釈液の量 (mL) / 希釈液の倍率 ※計算結果や情報等に関して当サイトは一切責任を負いません。 また個別相談は対応しません。 お客様の声 アンケート投稿 よくある質問 リンク方のだ。理科の計算問題では,わかりにくそ うに書いてある問題が多いから,式を書いて 整理することが,とても大切になってくるのだ。 しかも都合がよいことに,「水溶液と金属」のような,計算問題の理解がポイントになって18/7/ 次に、アルコール度数が分かっているアルコール水溶液に含まれるアルコールの質量を求める。 これは簡単で、 アルコール度数 x = アルコール質量% となる。 そこで、アルコール度数が10%のお酒が0ccあるとすると、 0 x (10/100) x = g gのアルコールが含まれていると計算できる。 という数字は、約08として計算すると簡単である。 0




質量パーセント濃度の計算問題集 応用編 Menon Network



基礎化学3 溶液
ここからあとの考え方が,「水溶液と金属」の問題における最も大切な考え方だ。 考え方に慣れるために,「こんにゃく」と「がんもどき」で「おでん」を作るという, おでん作り作業をやってみよう。下の図の が「こんにゃく」, が「がんもどき」だ。21/7/03 この式は、水より重い液体に適用される式です。 d = 1443/(1443 - Bh) d : 15℃水溶液の 比重(4℃の水を規準として) Bh : 15℃水溶液の ボーメ度 この式は元々 実験式ですし、また式の成り立ちから見ても計算結果の有効数字は 3桁か、せいぜい 4桁 と考えるべきです。 従って、15℃水溶液の Bh=130 とすると この水溶液の比重d は ; d = 1443/(1443-130) ≒



溶液の濃度計算 薬学 これでok




中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu




医療工学科の化学講義 16 溶液濃度計算問題演習 Life Chemistry




中1 理科 水溶液の濃度計算 ほぼ数学 Youtube




Gqkbqswdjmhsom




溶解平衡 溶解度積 の計算 問題と答え 化学計算の王道 大学受験の王道



3




Twitter 上的 Akiya Su 理科 質量パーセント濃度 溶質 溶媒 溶液と公式を覚えること 計算は難しくないが 割り算の筆算で小数点の位置がわからない人は先生に聞こう 中学理科 質量パーセント濃度 T Co Tri1p3fn72 Twitter



濃度算 薄める 高精度計算サイト




高校理論化学 溶液の濃度と調製 質量パーセント濃度 密度とモル濃度の単位換算 受験の月




中和の計算 基本 問題と答え 化学計算の王道 大学受験の王道



基礎化学3 溶液



中1理科 数学 食塩水の問題を動画でマスター 公式の覚え方と濃度の計算 マナブレイン
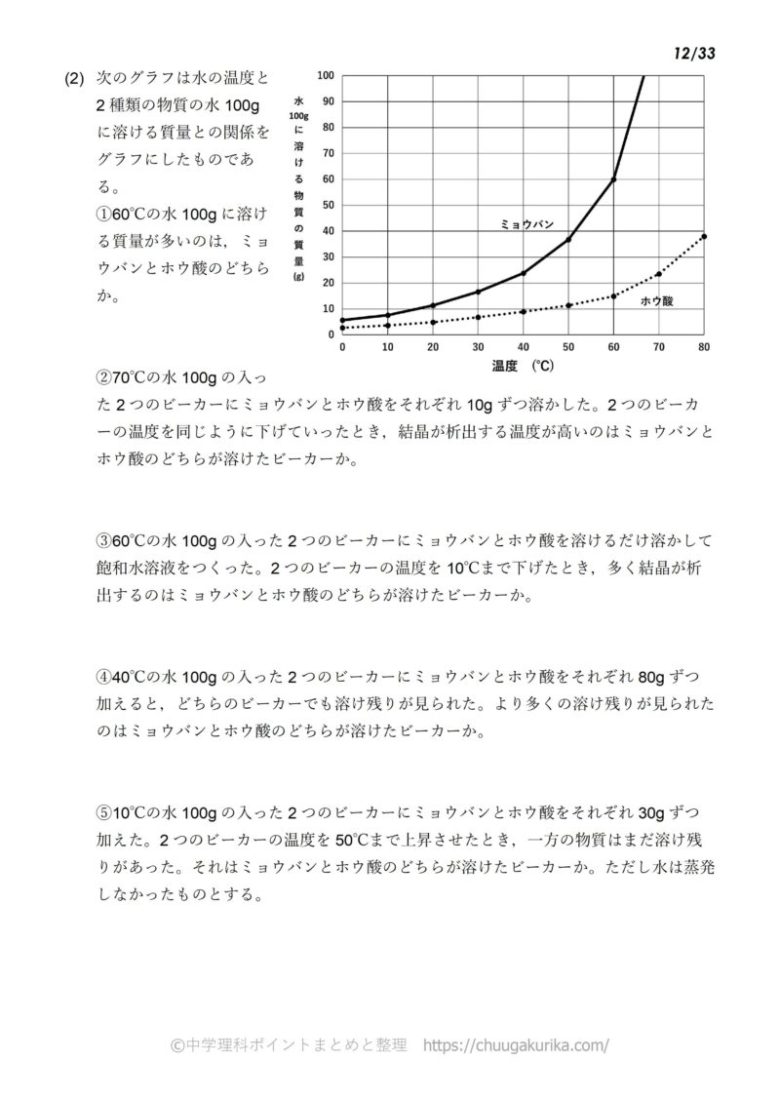



中1化学 溶解度の計算問題 中学理科 ポイントまとめと整理



中学1年生 理科 水溶液の性質 練習問題プリント 無料ダウンロード 印刷 ちびむすドリル 中学生




驚きの価格 中学受験 暗記カード 算数 国語 理科 社会 暗記カードセット 語学 参考書 Knowledge21 Com



こうして学べば必ずわかる 中学受験 理科




中学理科 水溶液の濃度と飽和 溶解度 偏差値40プログラマー




質量パーセント濃度の計算問題集 応用編 Menon Network



固体の溶解度 温度との関係 計算問題 溶解度曲線など 化学のグルメ
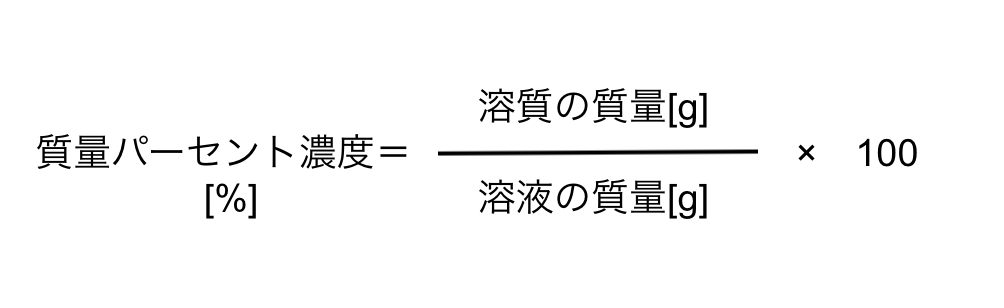



中1 理科 飽和水溶液 濃度 溶解度の重要ポイント 札幌市 西区 白石区 塾 学習塾 個別指導塾 マナビバ
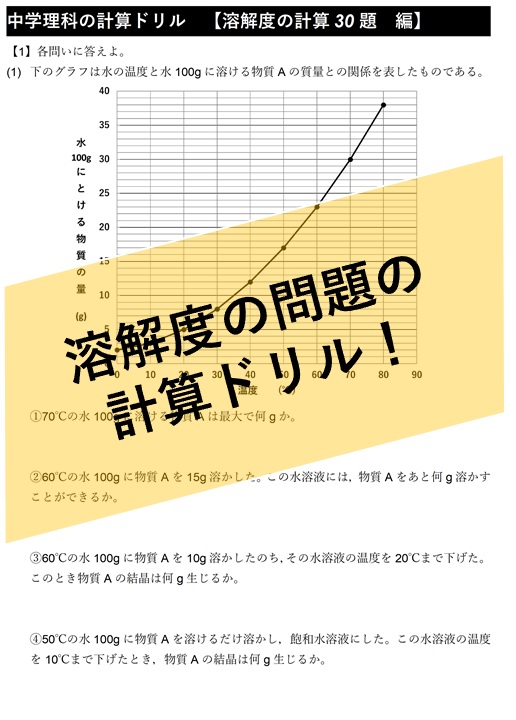



中1化学 溶解度の計算問題 中学理科 ポイントまとめと整理



化学のモル濃度計算の質問です 塩酸と硫酸は混合水溶液で 合 Yahoo 知恵袋




濃度の計算の人気動画を探索しましょう Tiktok



水溶液と質量パーセント濃度の計算問題 Hiromaru Note




理容師美容師国家試験の水溶液の計算で悩む方のために パターン3 最終日 地震とアスペルガー




中和の計算問題 無料で使える中学学習プリント




質量パーセント濃度の計算問題集 基本編 Menon Network



受験化学 10 溶解度の計算2 みかみの参考書ブログ
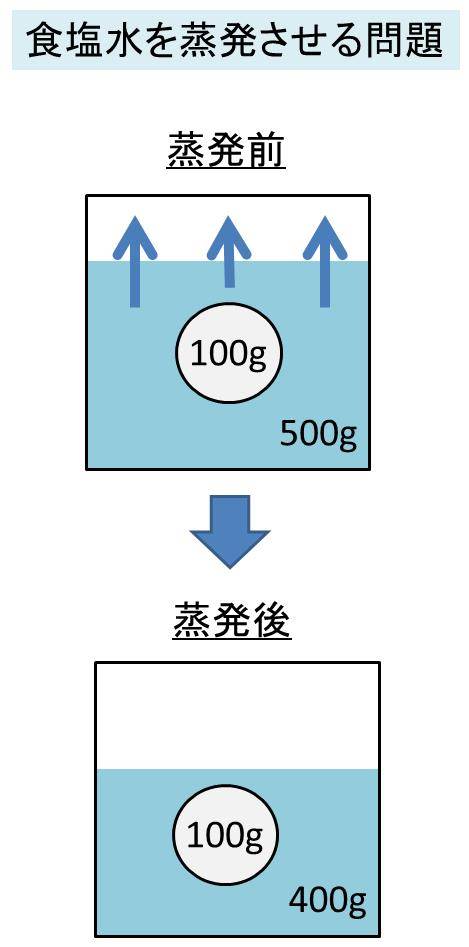



Spi 食塩水を蒸発させたときの濃度の計算方法 濃度算




中和の計算問題 無料で使える中学学習プリント




Pdf 濃度の計算ドリル45題 中学理科ポイントまとめと整理 オンラインショップ




質量パーセント濃度の計算問題集 応用編 Menon Network
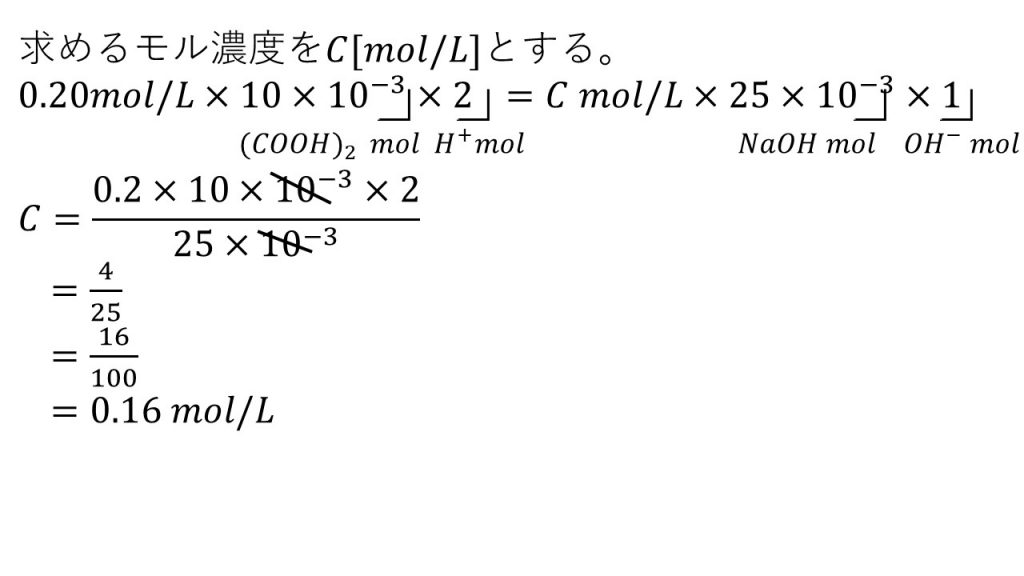



中和の計算 基本 問題と答え 化学計算の王道 大学受験の王道




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく



Gqkbqswdjmhsom




電気分解の計算 問題と答え 化学計算の王道 大学受験の王道




中学受験理科講座 水溶液の濃さと溶解度



中1化学 水溶液 濃度 中学理科 ポイントまとめと整理




中学受験理科講座 水溶液の濃さと溶解度



水溶液と質量パーセント濃度の計算問題 Hiromaru Note




高校化学基礎 濃度の計算 練習編 映像授業のtry It トライイット



酢酸水溶液の電離度の計算について 問題文の酢酸水溶液のh が2 Yahoo 知恵袋



中1 理科 飽和水溶液 濃度 溶解度の重要ポイント 札幌市 西区 白石区 塾 学習塾 個別指導塾 マナビバ



美容師国家試験 消毒法計算 公式を使わず簡単攻略 美容学校のセンセイが教える 美容師国家試験筆記対策




濃度計算を素早く 化学がちょっとだけ好きな社労士




中学1年生 理科 水溶液の性質 練習問題プリント 無料ダウンロード 印刷 ちびむすドリル 中学生




酸と塩基 Phの計算 酸性水溶液 ブリリアンス化学 Youtube
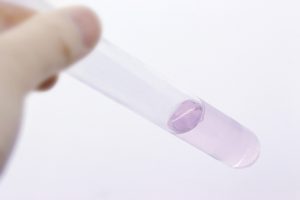



中1理科 水溶液 濃度の計算が10分で理解できる たけのこ塾 勉強が苦手な中学生のやる気をのばす




中1 理科 化学 濃度の計算方法 14分 Youtube
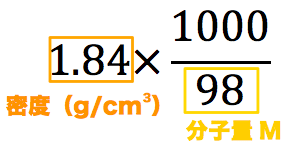



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ



受験化学 10 溶解度の計算2 みかみの参考書ブログ



中和滴定の計算の時に物質が水溶液の時のみ僕が 1 出してるような計算が出 Yahoo 知恵袋




モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ



溶質を求める




Pdf 濃度の計算ドリル45題 中学理科ポイントまとめと整理 オンラインショップ
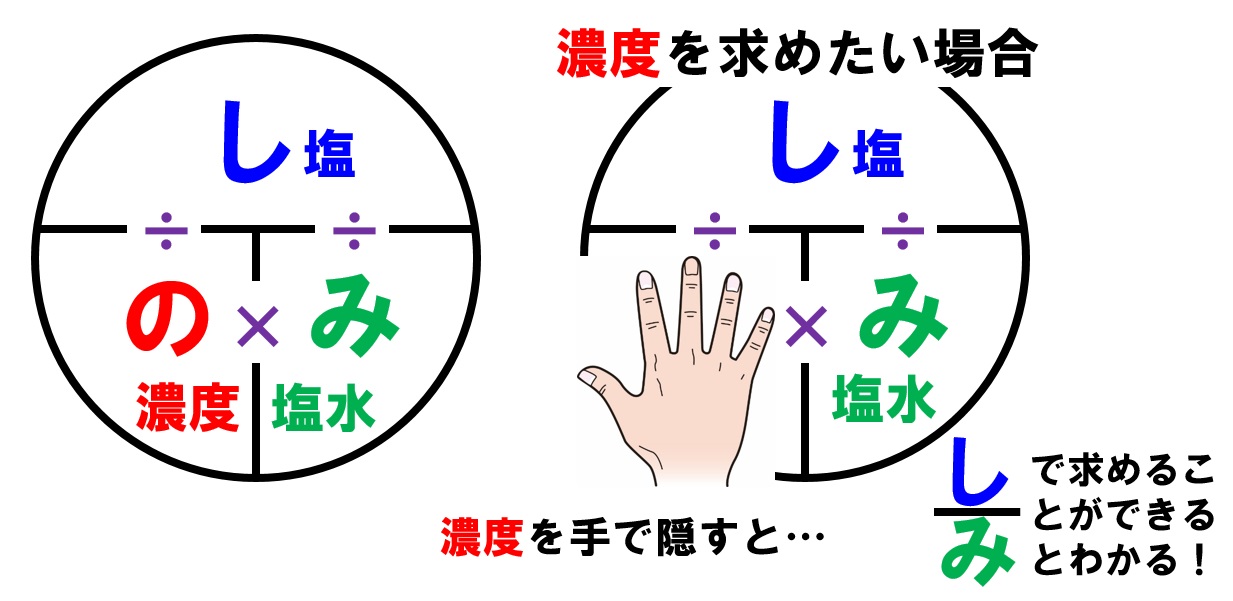



中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu




高校理論化学 食酢中の酢酸のモル濃度と質量パーセント濃度 受験の月




理容師美容師国家試験の水溶液の計算で悩む方のために パターン2 地震とアスペルガー




中1理科 3分でわかる 飽和水溶液 溶解度 溶解度曲線とは Qikeru 学びを楽しくわかりやすく
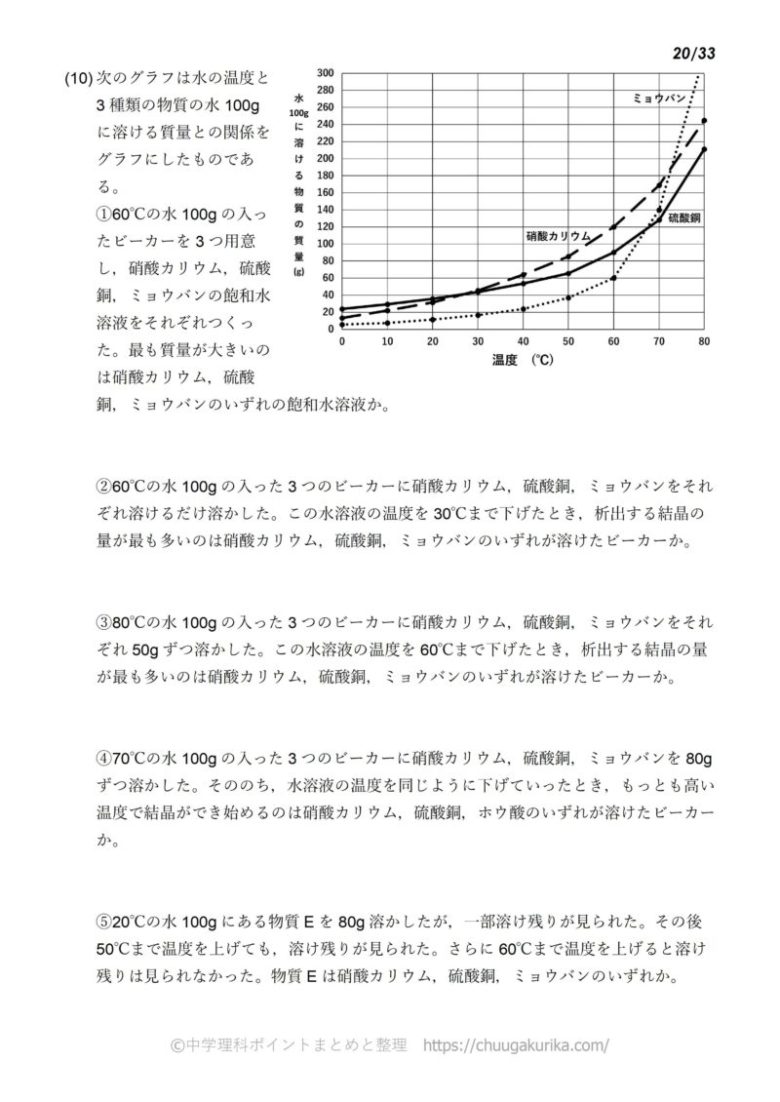



中1化学 溶解度の計算問題 中学理科 ポイントまとめと整理




4 6 溶液の濃度 おのれー Note



1




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




Pdf 濃度の計算ドリル45題 中学理科ポイントまとめと整理 オンラインショップ
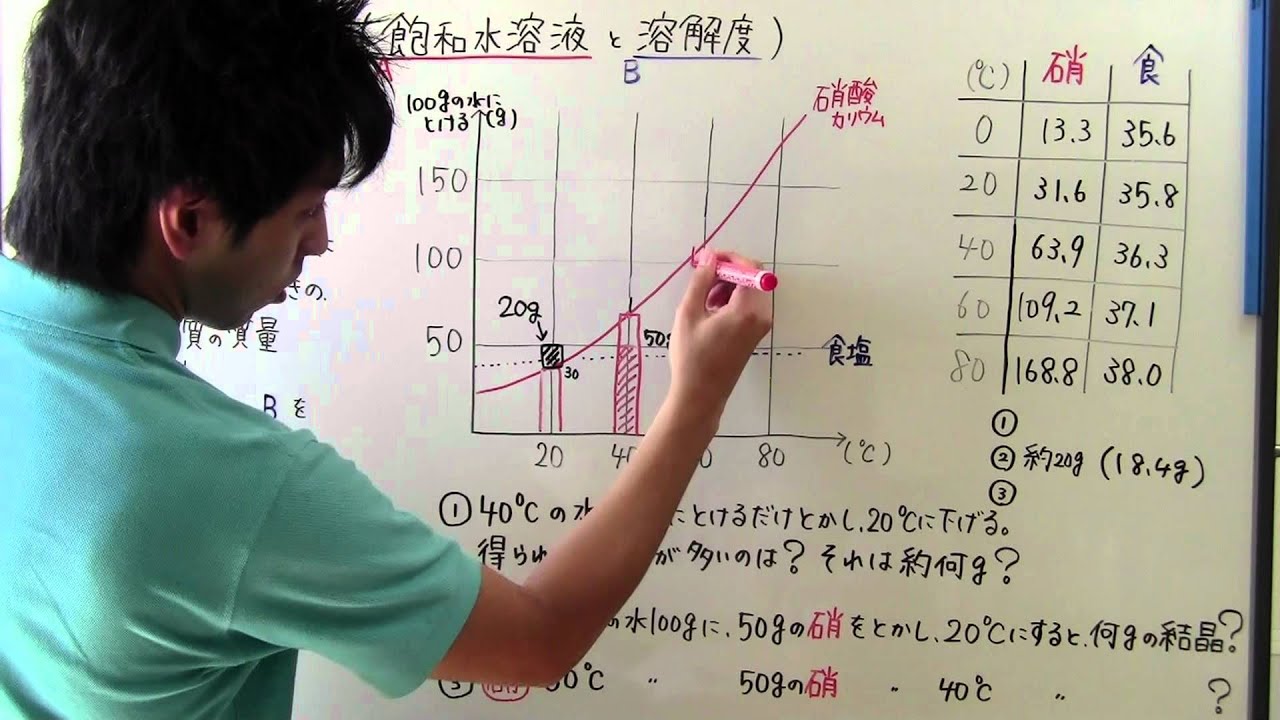



中1 理科 中1 34 飽和水溶液 溶解度 Youtube
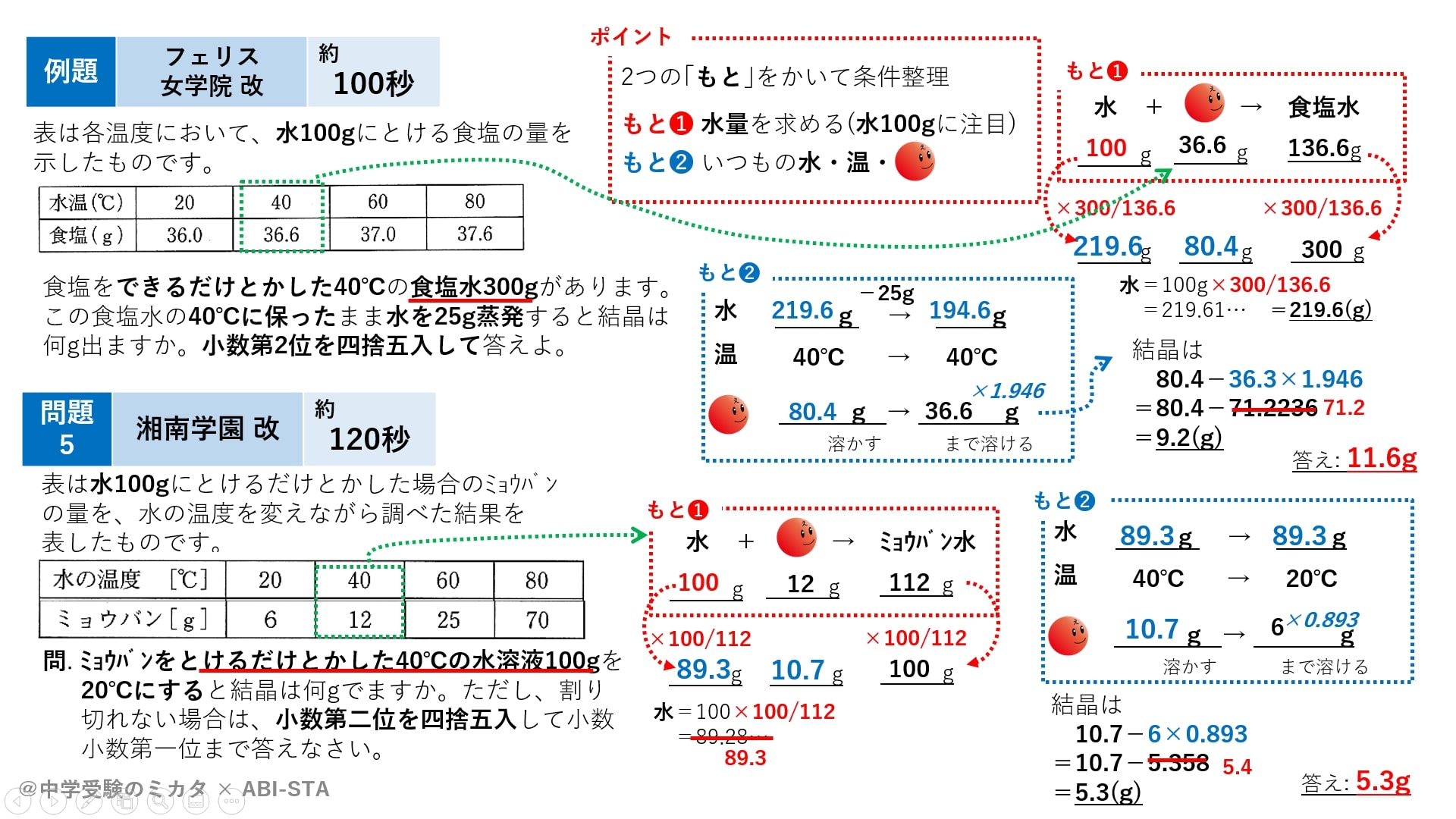



化学 21 10 飽和水溶液の溶解度計算
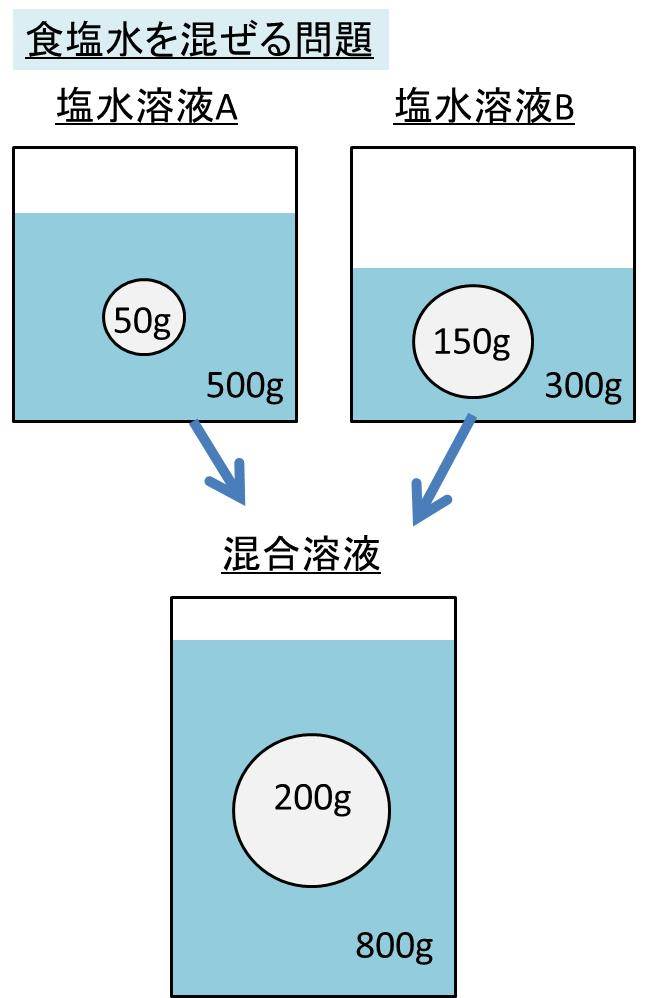



Spi 異なる濃度の食塩水を混ぜる問題の計算方法 濃度算
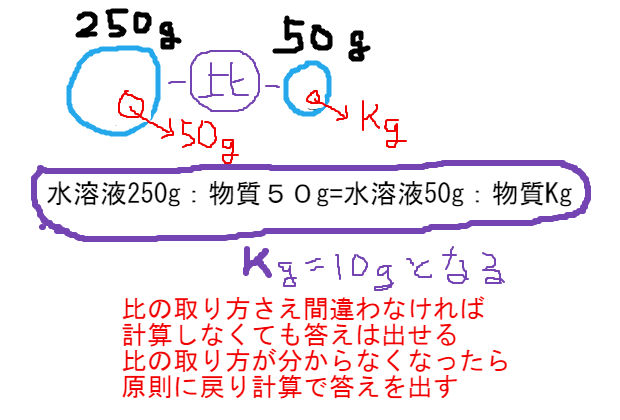



水溶液濃度 水を蒸発させたときの物質の質量計算 中学 数学 理科の復習サイト



医療工学科の化学講義 16 溶液濃度計算問題演習 Life Chemistry
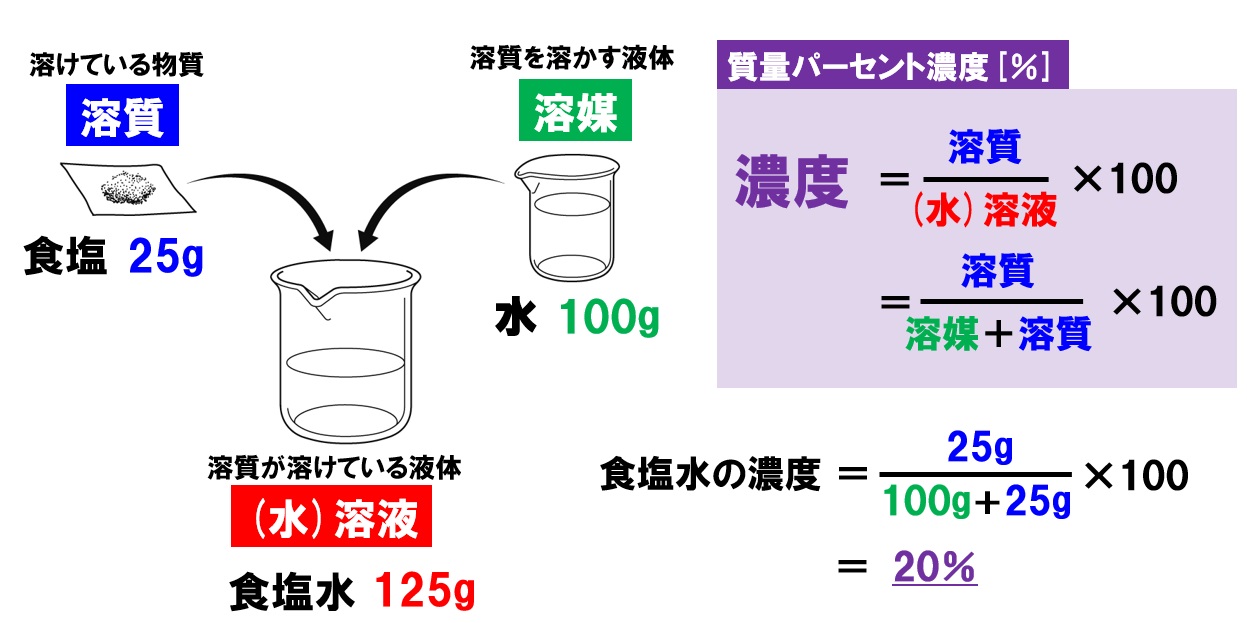



中1理科 水溶液と濃度 水溶液の性質と濃度計算 Pikuu
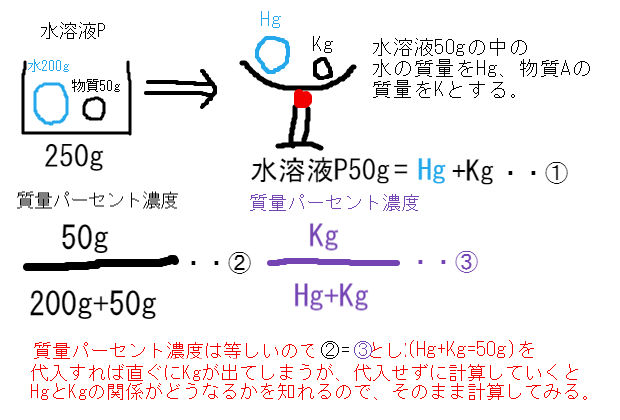



水溶液濃度 水を蒸発させたときの物質の質量計算 中学 数学 理科の復習サイト




理科 水溶液の計算 Youtube




中学1年生 理科 水溶液の性質 練習問題プリント 無料ダウンロード 印刷 ちびむすドリル 中学生
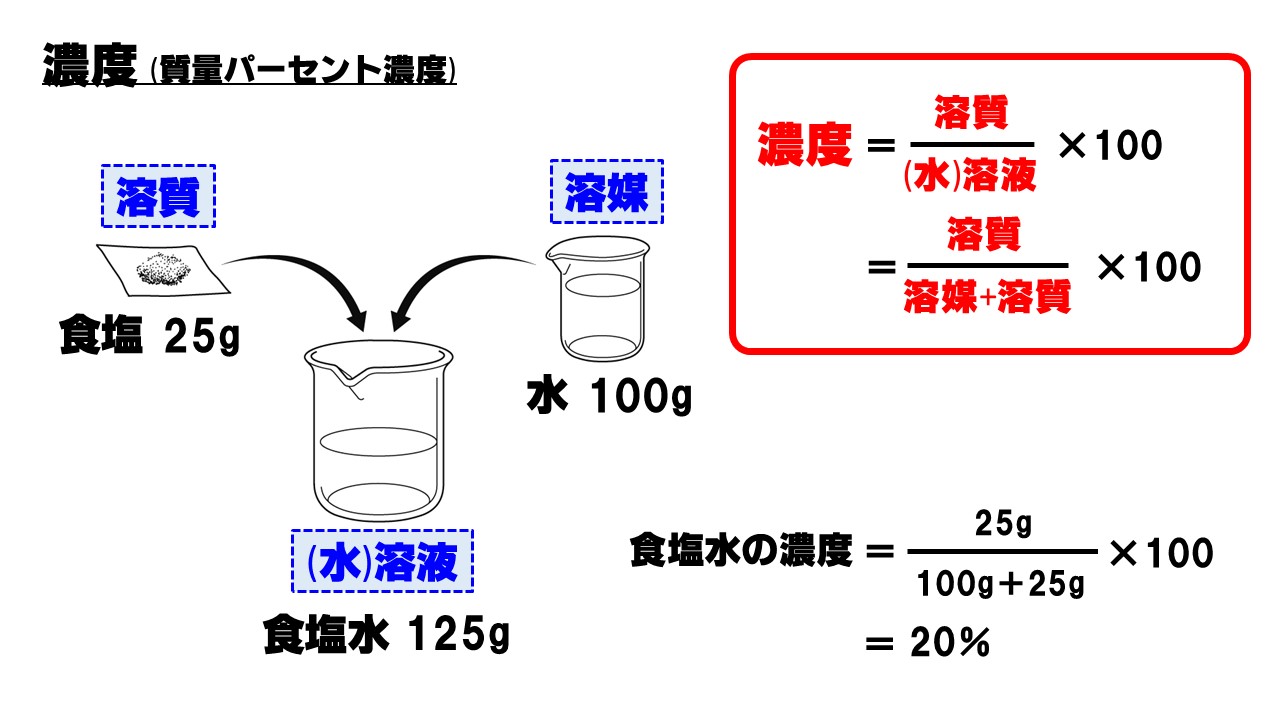



中1理科 濃度 質量パーセント濃度 のポイント Examee




理科 中1 27 質量パーセント濃度 Youtube




濃度の計算の人気動画を探索しましょう Tiktok




化学 水溶液の希釈 Youtube



濃度の応用




濃度の計算が苦手な人必見 公式と練習問題を元製薬会社研究員がわかりやすく解説 ページ 3 4 Study Z ドラゴン桜と学ぶwebマガジン



1



0 件のコメント:
コメントを投稿